Сердце можно представить в виду «двух взаимодействующих насосов»: правое сердце перекачивает кровь через лёгкое, левое - через периферические органы. Каждый «насос», в свою очередь, имеет по две сокращающихся камеры: предсердие и желудочек.
Сердечная мышца включает в себя три основных типа мышечной ткани: миокард предсердий, миокард желудочков и атипический миокард проводящей системы сердца.
Волокна проводящей системы содержат мало миофибрилл и сокращаются слабо. Основной их функцией является автоматическая генерация импульсов и проведение их к сократительному миокарду предсердий и желудочков.
Предсердия отделены от желудочков фиброзной перегородкой, имеющей высокое сопротивление. Поэтому в желудочки импульсы возбуждения передаются через специальный атриовентрикулярный пучок волокон проводящей системы, диаметром в несколько миллиметров. Это позволяет предсердиям сокращаться несколько раньше желудочков.
 Структура поперечного анатомического среза миокарда предсердий состоит из двух слоёв: поверхностного, общего для обоих предсердий, и глубокого, раздельного для каждого из них. В первом содержатся мышечные волокна, расположенные поперечно, а во втором - два вида мышечных пучков: продольные, которые берут начало от фиброзных колец, и круговые, выполняющие функции сфинктера, петлеобразно охватывая устья вен, впадающих в предсердия,.
Структура поперечного анатомического среза миокарда предсердий состоит из двух слоёв: поверхностного, общего для обоих предсердий, и глубокого, раздельного для каждого из них. В первом содержатся мышечные волокна, расположенные поперечно, а во втором - два вида мышечных пучков: продольные, которые берут начало от фиброзных колец, и круговые, выполняющие функции сфинктера, петлеобразно охватывая устья вен, впадающих в предсердия,.
Миокард желудочков состоит из различных по длине и толщине пучков мышечных волокон (миофибрилл), которые объединяются в структуры более высокого порядка, имеющие в плоскости поперечного сечения вид пластинки. Миокардиальные пластинки отделены друг от друга прослойками соединительной ткани и во всех участках сердечной стенки представляют собой закономерно упорядоченные самостоятельные единицы морфологического строения миокарда. Пучки волокон миокарда зачастую плавно переходят из одной миокардиальной пластинки в другую, связывая их. Следовательно, миокардиальные пластинки – это не изолированные образования, а взаимосвязанные, ступенчато переходящие друг в друга структуры. Такие переходы осуществляются в среднем через 1–3 мм.
Расположение миокардиальных пластинок имеет свои закономерности. Большей своей плоскостью они, как правило, ориентированы параллельно друг другу и поверхности стенок желудочков. Это обеспечивает достаточно свободное их скольжение при сокращении сердца и уменьшает непроизводительные энергетические расходы. Поэтому пластинки следует признать морфологическими структурами, формирующими условия для наиболее оптимального взаимодействия пучков волокон при структурной перестройке миокарда.
 Мышечное волокно представляет собой сложное многоядерное образование, содержащее 1000-2000 более тонких поперечно исчерченных волокон (миофибрилл) диаметром 1-2 мкм, которые раздваиваются и сливаются вновь, создавая разветвлённую сеть. Сердечная мышца выступает как синцитий с ответвляющимися связанными между собой клетками. Синцитий – это многоядерное протоплазматическое скопление клеток (рис. IV-1).
Мышечное волокно представляет собой сложное многоядерное образование, содержащее 1000-2000 более тонких поперечно исчерченных волокон (миофибрилл) диаметром 1-2 мкм, которые раздваиваются и сливаются вновь, создавая разветвлённую сеть. Сердечная мышца выступает как синцитий с ответвляющимися связанными между собой клетками. Синцитий – это многоядерное протоплазматическое скопление клеток (рис. IV-1).
Однако миокард не является подлинным анатомическим синцитием, так как клетки миокарда (кардиомиоциты) на самом деле отделены друг от друга в миофибриллах соответствующими сарколеммами продольно, а концы каждой клетки - плотными структурами, вставочными дисками, которые являются продолжением сарколеммы (рис. IV-2). Тем не менее, сердечная мышца функционирует как синцитий: при надпороговом раздражении в любой отдельной точке миокарда возникает волна деполяризации, за которой следует сокращение всего миокарда.

Рисунок IV-2. Микрофотография сердечной мышцы, полученная при помощи электронного микроскопа.
Описание строения миокарда желудочков, представляющее его в виде непрерывных пучков мышечных волокон от основания к верхушке, не соответствует истине, поэтому не может быть использовано для оценки архитектоники сердца.
Для справки: термин архитектоника состоит из двух слов греческого происхождения : ἀρχι (archi) — главный и τεκτον (tektos) — строить, возводить, что в прямом переводе означает «главное устроение» или основной принцип построения, общую систему связей между отдельными частями целого.
Целостная конструкция миокарда на макро- и микроскопическом уровне представляет сложную топографическую систему пучков волокон различной выраженности, ориентированных в различных направлениях и имеющих разнообразные связи между собой.
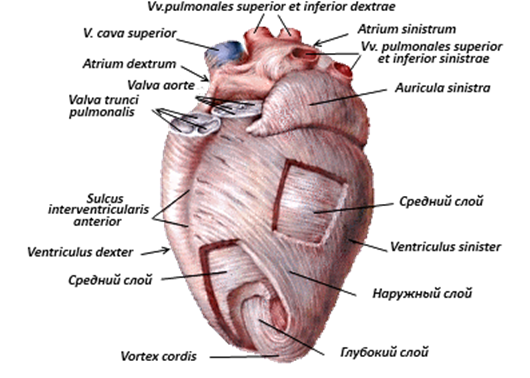
Рисунок IV-3. Анатомия сердца.
В стенке желудочков не удалось обнаружить чётких морфологических критериев, позволяющих разделить миокард на отдельные слои, поэтому такое разделение является весьма условным [58,59].
В миокарде можно выделить две группы пучков волокон. Одна группа - те, которые принадлежат обоим желудочкам и объединяют их в одно целое. Вторая принадлежит только одному из желудочков. Такие морфологические особенности конструкции миокарда позволяют обеспечивать, с одной стороны, сочетанную работу желудочков по выбросу крови в условиях нормальной гемодинамики, а в случае необходимости в каждом из желудочков имеется свой функциональный резерв мышечной ткани, который может изолированно реагировать и обеспечивать компенсацию выброса повреждённого желудочка.
Субэпикардиальный слой начинается в области атриовентрикулярных фиброзных отверстий, спускается преимущественно косо влево и вниз и через верхушку сердца ("водоворот", vortex cordis) уходит на внутреннюю поверхность стенки желудочков (рисунок IV-5), где продолжается в субэндокардиальном слое. Толщина поверхностного слоя незначительна и примерно равна 1–1,5 мм.
Главным признаком, по которому субэпикардиальная группа мышечных волокон выделена в отдельный поверхностный слой – это значительное отличие их ориентации от лежащих глубже. Изучение хода волокон показало, что поверхностные волокна начинаются в области атриовентрикулярных отверстий желудочков, атриовентрикулярной части межжелудочковой перегородки, устьев аорты и лёгочного ствола.
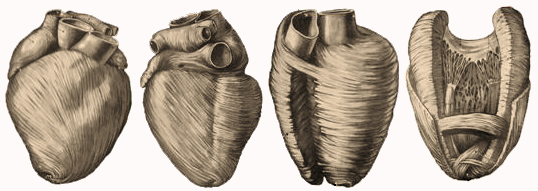
Рисунок IV-4. Направление волокон миокарда в слоях желудочков.
Спереди слой наиболее поверхностно расположенных волокон охватывает путь оттока ПЖ, в области передней межжелудочковой борозды они частично переходят на ЛЖ, продолжаются по его переднебоковой стенке, относительно которого они имеют циркулярное направление, делают один завиток и переходят в «водоворот» (vortex cordis).
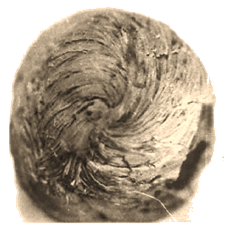
Рисунок IV-5. Оригинальный препарат мышцы сердца со стороны верхушки (по Коваленко В.Н., 2002)
Пучки волокон, начинающиеся от переднебоковой части левого атриовентрикулярного отверстия, идут косо, охватывая в основном ЛЖ. Небольшая часть этих волокон, которые начинаются непосредственно от боковой части левого атриовентрикулярного отверстия, переходит на ПЖ и заворачивает в водоворот.
Сзади волокна поверхностного слоя начинаются в области задних частей атриовентрикулярных отверстий правого и левого желудочков и имеют циркулярное направление относительно пути притока и оттока. Заканчиваются эти волокна в нижней половине передней стенки левого желудочка. Спиралеобразный ход этих пучков в области задних стенок желудочков характеризуется наибольшим диаметром и наименьшим шагом по сравнению с остальными частями стенок желудочков. По мере приближения к верхушке сердца угол их наклона увеличивается, то есть ход их становится более вертикальным.
Традиционно, поверхностный слой миокарда принято называть «наружной косой мышцей». Но этот термин неверен, поскольку цельная мышца должна иметь иные анатомические и физиологические характеристики.
Средний слой мускулатуры желудочков состоит из пучков волокон в большинстве своём имеющих спиралеобразный ход, однако их угол изменяется, в зависимости от расположения, как по глубине залегания, так и по отдалённости от основания к верхушке желудочка. Пучки волокон этой группы начинаются в области задних частей атриовентрикулярных отверстий желудочков и имеют направление, близкое к циркулярному. По мере углубления в сердечную стенку волокна постепенно приобретают более пологое направление, и примерно в середине стенки ход их становится циркулярным относительно длинной оси желудочка. Изменение направления пучков волокон из косого в циркулярное осуществляется настолько плавно, что границу между ними провести невозможно. А затем внутренние, углубляясь от середины стенки, вновь возвращаются к параллельному продольной оси, но уже противоположному, направлению.
Изучение ориентации пучков волокон миокарда показало, что слой “чисто” циркулярных волокон, традиционно называемой «циркулярной мышцей», выражен незначительно. Они наблюдаются только в середине стенки желудочков. Поэтому более надёжным является разделение основной массы миокарда на два приблизительно равных по толщине слоя: наружный и внутренний.
Толщину внутреннего слоя волокон определяют от середины циркулярного слоя до папиллярно-трабекулярного аппарата ЛЖ. Внутренние пучки волокон идут в виде спиралей обратного хода по сравнению с наружными. Глубокий слой состоит из пучков, поднимающихся от верхушки сердца к его основанию. Они многократно расщепляются и снова соединяются, образуя различной величины петли. По мере приближения к эндокарду эти пучки приобретают более крутое направление и переходят в трабекулы. Пучки волокон здесь ориентированы параллельно длинной оси в виде отдельных анатомических структур папиллярно-трабекулярного аппарата. Более короткие из этих пучков не достигают основания сердца, а более мощные из них, связанные отчасти и со средним, и с наружным слоем, выступают в полость желудочков свободно, образуя различной величины конусовидные сосочковые мышцы.
Сокращение папиллярных мышц приводит к натяжению створок атриовентрикулярных клапанов.
Ход пучков волокон в левой половине межжелудочковой перегородки существенно не отличается от расположения их в стенке ЛЖ. Волокна, составляющие межжелудочковую перегородку, имеют такую же ориентацию, что и волокна соответствующих частей стенок желудочков.
Обобщение результатов биометрического анализа желудочков сердца позволяет сделать следующее заключение. Стенка сердца по поверхности и в глубине имеет различные биомеханические условия сокращения. К ним можно отнести разную кривизну поверхности сердца, разнонаправленную ориентацию пучков волокон миокарда, распределение массы по стенкам сердца (толщину). Особенности распределения и направления пучков волокон миокарда у верхушки и основания определяют продольное укорочение в области верхушки и циркулярное - у основания.
 J.Ross и соавторы (1968) при рассмотрении проблемы моделирования желудочков сердца отметили, что «для построения точной модели требуется информация о последовательных изменениях формы полости и одновременных изменениях толщины сердечной стенки в течение сердечного цикла, а также о характере распределения напряжения». Последнее напрямую связано с ориентацией пучков волокон миокарда, как минимальных носителей силы сокращения сердца, которые могут служить эквивалентами элементарных силовых векторов.
J.Ross и соавторы (1968) при рассмотрении проблемы моделирования желудочков сердца отметили, что «для построения точной модели требуется информация о последовательных изменениях формы полости и одновременных изменениях толщины сердечной стенки в течение сердечного цикла, а также о характере распределения напряжения». Последнее напрямую связано с ориентацией пучков волокон миокарда, как минимальных носителей силы сокращения сердца, которые могут служить эквивалентами элементарных силовых векторов.
Для справки: кинематика - это раздел механики, который изучает перемещение тела (объекта) в пространстве и времени, не рассматривая причин, его вызвавших, и использует при этом векторные величины, характеризующие не только положение данного тела (объекта), но и направление его движения.
Итак, задачей кинематики сердца является оценка его работы через хронологическую последовательность:
- сокращения мышечных волокон;
- трансформации камер сердца;
- направления векторов силы сокращения миокарда на протяжении сердечного цикла.
В мировом научном сообществе нет единого мнения по последовательности сокращения мышечных волокон и изменения геометрии камер сердца.
Сегодня в кардиологии наряду с известной классической концепцией трёхслойного строения миокарда желудочков параллельно существует и новая, оценивающая архитектонику сердца в виде развёрнутой полосы. Остановимся на принципиальных положениях этих подходов оценки строения и функционирования миокарда.
Согласно классической теории, мышечная ткань желудочков имеет три слоя: наружный косой (субэпикардиальная мышца), средний круговой (циркулярная мышца) и внутренний продольный (субэндокардиальная мышца). Наружный слой является общим для обоих желудочков, круговой и продольный – раздельные для каждого. Сокращение субэпикардиального слоя желудочков вызывает поворот верхушки сердца вокруг его продольной оси вправо, во время которого каждая из полостей желудочков отчётливо делится на два отдела: путь притока и путь оттока. При сокращении среднего циркулярного слоя полости желудочков уменьшаются в диаметре и их наружные стенки движутся внутрь. Волокна внутреннего продольного слоя, являясь продолжением наружного косого, после разворота на верхушке на 180° устилают внутреннюю поверхность сердца, входя в трабекулы и сосочковые мышцы сердца.
По классическим представлениям, функции миокарда слагаются из сокращения и расслабления. В систолу желудочков, (в фазы изоволюмического сокращения, быстрого и медленного изгнания), последовательно происходит уменьшение объёма полости желудочка в поперечнике (циркулярный слой) и укорочение его длинной оси (наружный косой и внутренний продольный слои). Эти изменения присущи сокращению миокарда желудочков (активная фаза). А в диастолу (в фазы изоволюмического расслабления, быстрого, медленного наполнения) в процессе плавной релаксации, происходит увеличение объёма полостей желудочков и удлинение их продольных осей.
При таком подходе прослеживаются следующие слабые моменты:
- Каждый мышечный слой рассматривается как цельная мышца, из чего следует, что при возбуждении должно происходить её сокращение по всей длине от основания до верхушки. На самом деле, слои состоят из отдельных пучков, выполняющих свою работу в определённой хронологической последовательности. Независимо от того, о каком бы слое мы не говорили, последний возбуждается не одновременно по всей длине, а постепенно, по мере возбуждения той или иной группы мышечных волокон. Из этого вытекает, что субэпикардиальный слой может частично сократится в базальном отделе, оставаясь расслабленным на верхушке.
- Укорочение сердца по длинной оси связывают с сокращением «наружной косой» и «внутренней прямой мышц», являющихся по сути одним слоем мышечных волокон, только имеющих противоположное направление. Толщина этого слоя незначительна (не более 1-1,5 мм) и недостаточна для выполнения такой работы.
- Диастолическое наполнение расценивается как пассивный процесс. Существует достаточно доказательств, что диастола такой же активный процесс, как и систола, и осуществляется при сокращении некоторых мышечных слоёв.
Теория развёрнутой полосы. В 1957 г. F. Torrent-Guasp (1931 - 2005) [3,131] привёл доказательства, что сердечная мышца сформирована одним слоем миокарда. Он рассматривал сердце как мышечную полосу, которая начинается в устье лёгочной артерии (ЛА), делает два оборота и заканчивается в устье аорты (Ао). Он сравнивает эту полосу с верёвкой, имеющей спиралевидный ход волокон. Действительно, после анатомического препарирования, она похожа на «полосу» или «ленту». На вопрос о том, что его привело к подобным выводам, F. Torrent-Guasp ответил: «Следуйте за волокном, и вы узнаете его путь».
Данный подход даёт объяснение анатомическим причинам различия толщины свободной стенки левого и правого желудочков. Свободная стенка ЛЖ состоит из двух петель и является более толстой, чем свободная стенка правого желудочка (ПЖ), которая представлена только одной петлёй.
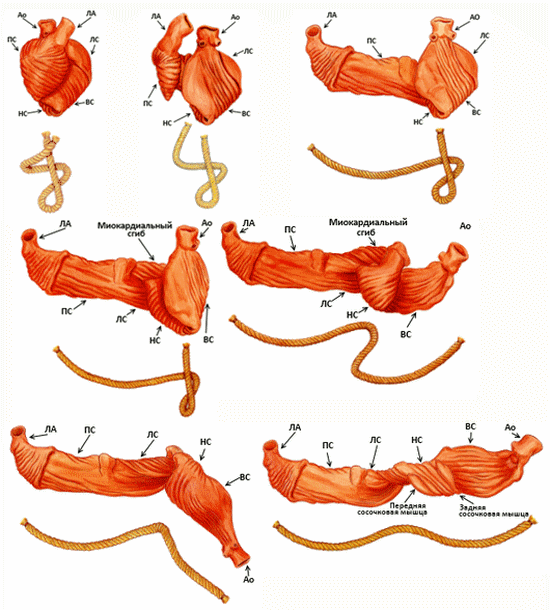
Рисунок IV-6. Последовательность разворачивания миокарда желудочков в полосу (по F. Torrent-Guasp).
Изучение «развёрнутой полосы миокарда желудочков», позволило по-новому оценить строение и функционирование миокарда, который свёрнутый в виде спирали, образует два цикла: базальный и верхушечный, каждый из которых делится на два сегмента. Широкая её часть названа основным или базальным циклом (первый виток спирали), за которой следует более узкая часть, завёрнутая во второй виток спирали, образующий верхушку сердца, он назван апикальным циклом.
Развёрнутый базальный цикл, формируемый свободной стенкой правого и левого желудочков, состоит из правого (ПС) и левого (ЛС) сегментов. Направляясь от корня ЛА к центральному сгибу, его волокна огибают правую и левую стороны сердца в высоком и среднем отделах. Длинная ось желудочков перпендикулярна данному слою миофибрилл.
Верхушечный цикл имеет продолжительность от сгиба до корня аорты. Нисходящий сегмент (НС) цикла начинается внутренними волокнами перегородки и задней стенки левого желудочка после поворота полосы по центральному сгибу на 180°, и направляется вертикально к верхушке, условно параллельно длинной оси желудочков. Переход нисходящего сегмента в восходящий (ВС) происходит под углом около 90°. Нисходящий и восходящий сегменты полосы миокарда граничат по задней сосочковой мышце, принадлежащей нисходящему сегменту. Восходящий сегмент заканчивается у корня аорты. Развёрнутая часть апикального цикла завершает превращение миокарда в цельную полосу (рис. IV-6).
Верхушка сердца – достаточно мощное мышечное образование преимущественно принадлежит левому желудочку. Она состоит не только из субэндо- и субэпикардиальных волокон, которые формируют «винтовой» ход вокруг центрального туннеля верхушки («vortex cordis»), но и нисходящего и восходящего сегментов апикального цикла, являющиеся продолжением мощного срединного слоя.
Винтовая модель позволяет четырёхмерно (с учётом шкалы времени) оценить расположение и взаимодействие различных слоёв миокарда. По сути, она характеризует хронологическую последовательность и направление силовых векторов при сокращении сегментов мышцы на протяжении сердечного цикла.
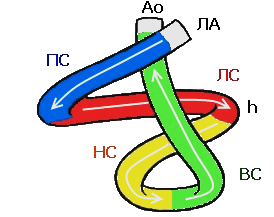
Рисунок IV-7. Винтовая модель миокарда.
Поочерёдная активность каждого из четырёх сегментов приводит к четырём основным движениям миокарда: сужению, укорочению по длинной оси, удлинению и расширению. При этом базальные отделы сердца осуществляют движение вверх и вниз, а верхушка остаётся практически неподвижной.
Ещё Пуркинье в 1843 году заметил, что верхушка сердца на протяжении сердечного цикла остаётся малоподвижной, в то время как предсердно-желудочковая плоскость активно перемещается вдоль продольной оси к верхушке в систолу и обратно в диастолу.
Какое же объяснение данному феномену дают авторы и сторонники однополосного строения миокарда? По их мнению, «точками опоры сердца являются аорта и лёгочная артерия, с одной стороны, и сама кровь в полости желудочков - с другой. Динамическая «точка опоры» сформирована инерцией определённого объёма крови, находящегося в полости желудочков сердца (внутрижелудочковый объём крови - «hemoskeleton», каркас крови). Преобладающие продольные волокна нисходящего сегмента вместе с исходно большим «каркасом крови» (конечно-диастолический объем ЛЖ) сокращаясь, приводят к смещению вниз основания желудочков».
Проанализируем сказанное. Действительно, основание сердца фиксируется в организме с помощью крупных выносящих и вносящих сосудов. Но парадокс заключается в том, что не свободная верхушка смещается к фиксированному основанию, а наоборот. Чтобы дать этому объяснение авторы предлагают версию о гемоскелетоне.
С моей точки зрения, это очень слабая, плохо продуманная мысль. Даже сам термин подобран очень неудачно. Скелет, каркас – это некое устойчивое образование, на базе которого создаются те или иные надстройки. Именно в последних и совершаются какие-то процессы, на затрагивая сам остов. Кровь это неустойчивая жидкая среда. На протяжении сердечного цикла меняются не только её объём, но и форма содержащего её «сосуда», каковым является сердце. Следуя логике авторов можно воздух в раздутом шарике назвать «аэроскелетоном».
Хочу напомнить, что инерцию связывают с массой тела, на которую действует некая сила, для придания ей ускорения. У сердечной мышцы хватает силы, чтобы изгонять в систолу бóльшую часть крови, хорошо справляясь с её инерцией. Исходя из контекста, следует предположить, что речь идёт не об инерции, а о весе крови. Однако вес напрямую связан с силами гравитации: вес равен массе умноженной на ускорение силы тяжести свободно падающего тела (в данном случае на Земле). Проще говоря, кровь должна выполнять функцию гири, тянущей верхушку к Земле и не позволяющей ей подтягиваться к основанию.
Это можно в некоторой степени принять, если верхушка сердца всегда будет находиться к Земле ближе, чем основание. Однако человек меняет положение своего тела, что может приводить к совершенно иной ситуации, когда верхушка находится на уровне основания, и даже выше его. А в невесомости этот закон просто не буде действовать. Чересчур зыбка эта третья точка опоры, чтобы природа взяла её на вооружение.
F.Torrent-Guasp продекларировав, что надо следовать за волокнами, совершенно не дал никакого объяснения тому, что наряду с доминирующим направлением миофибрилл в каждом слое имеется огромное количество волокон с совершенно иным, зачастую противоположным направлением. Значит, при возбуждении того или иного слоя действуют силы, вектора которых имеют направление отличное от главного.
Проигнорировано существование наружного косого слоя, имеющего направление волокон, перпендикулярное базальным сегментам. Неслучаен и «водоворот» верхушки «закрученный» данной мышцей.
Творец ничего не создаёт случайно. Если это существует, то ему следует искать объяснение.
Какие же выводы? Классическая и новая теории не лишены недостатков и далеки от совершенства. Взяв лучшее из каждой и взаимно дополнив друг друга, можно более чётко оценить кинематику сердца.
В систолу базальные и средние сегменты левого желудочка смещаются внутрь полости по направлению к верхушке. Апикальные сегменты также движутся внутрь, но не к основанию сердца, а к условной точке – его динамическому центру, который расположен между второй и третьей частями длинной оси (69% расстояния от основания до верхушки). Все сегменты желудочка во время систолы направляются к этой точке под разными углами и с разной экскурсией. Наибольшее продвижение совершает основание сердца при почти полном его отсутствии в апикальных сегментах. В диастолу все сегменты миокарда расходятся центробежно от данной точки левого желудочка.
Разовьём эту мысль дальше, в сердце имеется некий центр динамического равновесия, являющийся ориентиром для всех силовых векторов. В систолу все вектора центростремительно направлены в эту точку. В диастолу, наоборот, вектора силы, формируемые иными мышечными слоями, направлены центробежно. В каждый момент в точке динамического равновесия пересекаются силы равной величины, но противоположного направления. Сила, направленная с одной стороны, уравновешивается противоположным вектором силы.
Однако верхушка, хотя и смещается к основанию, при этом совершает по сравнению с ним вдвое меньший путь. Такое выполнимо, только если верхушка будет зафиксирована какими-то силами в своей точке лучше, чем предсердно-желудочковая плоскость, и иметь больший силовой потенциал. Например, атлет может поднять штангу своего веса на вытянутые руки, но и может подтянуть себя на перекладине, используя ту же силу.
Что же удерживает верхушку в стабильном положении?
Приведу пример, запущенный вверх вращающийся пропеллер может долго оставаться в одной точке, пока на него не подействует какая-либо внешняя сила. Какие же силы «фиксируют» его в этой точке? По всему периметру данного пропеллера действуют центробежные силы, уравновешивая друг друга. До тех пор пока сила каждого из векторов будет равна силе противоположно направленного, пропеллер будет находиться в одной точке. Силовые вектора, как растяжки фиксируют его по всему периметру.
Теперь посмотрим на верхушку сердца (рис. IV-5). Vortex cordis, образованный субэпикардиальным слоем, очень напоминает вращающийся пропеллер. Такое расположение мышечных волокон удерживает верхушку как на растяжках, не позволяя ей существенно смещаться не только в стороны, но и по продольной оси.
Субэндокардиальный слой, являясь продолжением субэпикардиального, меняет своё направление на 180° и переходит на внутреннюю поверхность левого желудочка. Угол, под которым волокна данного слоя ориентированы, существенно отличается от ориентации волокон наружного косого слоя. Вероятно, эти слои, работая антагонистически, совместно участвуют в стабилизации верхушки.
Можно предположить, что разнонаправленность мышечных волокон одного слоя служит неким противовесом главным силам, влияя на устойчивость сердца и корригируя направление основных векторов силы. По сути, они выполняет задачу, аналогичную хвостовому пропеллеру вертолёта, стабилизирующему устойчивое положение, не позволяя ему раскрутиться.
Итак, подведём итог. При сокращении определённой группы мышц, формирующих доминирующий вектор силы, в то же время сокращаются многие волокна иного направления. Их задачей является стабилизация данного региона, создания некой «фиксированной точки», от которой происходит сокращение или растяжение данного мышечного слоя. В подвешенном органе, каковым является сердце, такой принцип позволяет сформировать наиболее оптимальные условия для изгнания крови в систолу и заполнения камер сердца в диастолу с наименьшими энергозатратами.
Хочу ещё раз напомнить, что на протяжении сердечного цикла миокард осуществляет четыре основных действия: в систолу – поперечное циркулярное сужение и укорочение по длинной оси, в диастолу – расширение и удлинение. Однако с помощью экспериментальных и современных диагностических методов - допплеровская визуализация тканей (tissue Doppler imaging – TDI), МРТ - доказано, что миокард сердца выполняет ещё два действия – скручивание и раскручивание [129].
Апикальный цикл состоит из нисходящего и восходящего сегментов «сердечной полосы», которые крестообразно пересечены в области верхушки, что приводит к возникновению противоположных эффектов при сокращении. От перекрёста на верхушке нисходящий и восходящий сегменты апикального отдела расходятся друг от друга под углом ≈90° и присоединяются к базальному отделу в различных точках. При совместном сокращении они подтягивают основание к верхушке, окорачивая длинную ось. При раздельном – происходит прокручивание базального отдела в ту или иную сторону [91].
Для справки: скручивание (twist) - круговое смещение точек на противоположных полюсах относительно друг друга. Это возможно, если полюса оси либо вращаются в противоположных направлениях, либо один полюс фиксирован или отстаёт в скорости вращения. Скручивание напоминает действие, совершаемое при отжимании воды из мокрого полотенца. Раскручивание (untwist) – действие противоположное скручиванию. Ротация (лат. rotātio) однонаправленное круговое, вращательное движение тела вокруг своей оси.
Круговое движение сердца принято оценивать в градусах со стороны верхушки по часовой или против часовой стрелки. Степень скручивания определяется по углу вращения базальных отделов относительно верхушки.
Первыми сокращаются косо направленные волокна нисходящего сегмента, при сокращении которых совершается вращение базального отдела против часовой стрелки. Одновременно с этим, продолжающий сокращаться наружный косой слой, проворачивает верхушку по часовой стрелке. В результате этого осуществляется скручивание сердца. Такое действие вызывает последовательно уменьшение сечения основания и изменение формы желудочков в виде сужения верхушки. Среднее значение угла скручивания ЛЖ в здоровой популяции составляет 5-13°.
Восходящий сегмент длиннее нисходящего. При сокращении нисходящие волокна, вращая основание сердца против часовой стрелки, «накручивают» волокна восходящего сегмента, накапливая в них дополнительный потенциал энергии.
Когда восходящий сегмент сокращается, происходит раскручивание сердца в результате вращения основания желудочка по часовой стрелке. Не исключено, что в этот момент, именно субэндокардиальный слой придерживает верхушку, прокручивая её в противоположном направлении.

Рисунок IV-8. Скручивание и раскручивание сердца при раздельном сокращении сегментов верхушечного цикла.
Движение сердца, как и всякого материального объекта, подчиняется основополагающим законам физики. Наиболее применимы для данной темы законы, заложенные в разделе механики. Механика – это наука о движении (и о равновесии) тел, а также о силах, вызывающих это движение.
Третий закон о движении, сформулированный Исааком Ньютоном, гласит, каждому действию есть равное направленное на него противодействие. Иными словами всякая сила не может действовать бесконечно, а всегда будет стремиться к нулю. Из этого следует, что сила действия, возникшая в систолу в результате сокращения сердечной мышцы, будет к концу диастолы сведена силами противодействия к своей начальной нулевой точке.
Сердце – уникальный полый орган, который не только удерживает кровь в своих полостях, но и за счёт активных действий, путём сдавления и растяжения, меняет её плотность. Плотность ткани формируется путём изменения её массы и объёма. Чем больше масса и меньше объём, тем больше плотность, и наоборот. Именно этот принцип и использует сердце в своей работе.
Кровь оказывает противодействие силам давления пропорционально своей плотности. Иными словами, не только стенка давит на кровь, но и кровь оказывает аналогичное давление на стенку, причём распределяя его равномерно по всей внутренней поверхности желудочка.
Несколько слов о трансмуральном давлении. Оно возникает при одновременном воздействии на стенку полого органа внутренних и внешних сил. Если внутренние силы преобладают над внешними, то стенка выпячивается кнаружи, и наоборот. Внутренние силы представлены преимущественно плотностью крови, внешние – упруго-эластичными свойствами стенки сердца, формируемыми, прежде всего, сокращением её слоёв.
Поскольку мышечные волокна сокращаются неодновременно, то давление, дополнительно полученное кровью при их сокращении, равномерно распределится по всей внутренней поверхности камер сердца. На тех участках, где мышца будет расслаблена, внутренние силы возьмут верх над внешними, что приведёт к выдавливанию стенки кнаружи, и региональному изменению геометрии камер сердца.
В результате градиента давления между внутренними и внешними силами на клапанном аппарате, его створки могут открываться или захлопываться, что используется при изгнании или присасывании крови.

Последовательность сокращения той или иной группы мышечных волокон напрямую зависит от времени их возбуждения. Если мы будем знать время и очерёдность прихода электрического импульса, вырабатываемого центром автоматизма, то сможем достаточно точно определить и последовательность сокращения миокарда. В этом нам может помочь электрокардиограмма и векторкардиограмма.
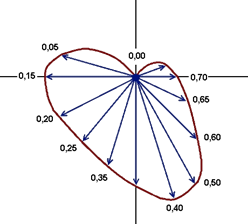
Рисунок IV-9. Векторная петля деполяризации желудочков во фронтальной плоскости (по Mann, 1920 г.)
По электрокардиограмме начальная часть комплекса QRS (зубец q) оценивает деполяризацию перегородки (≈0,01мс), восходящее колено зубца R – правого желудочка (≈0,025мс), нисходящее колено зубца R – верхушки и левого желудочка (≈0,03мс), конечная часть комплекса QRS (зубец s) связывают с деполяризацией базального отдела левого желудочка (≈0,01мс).
Последовательность возбуждения миокарда на протяжении сердечного цикла наглядно отображена на векторной петле деполяризации (рисунок IV-9). Максимальный вектор деполяризации сердца направлен влево, вниз, вперёд. Вектор деполяризации межжелудочковой перегородки (зубец q) направлен вправо, вниз, вперёд. В норме начало электрической активации базальной области миокарда совпадает по времени с конечной частью нисходящей линии R-волны или вершиной зубца s на ЭКГ. Вектор деполяризации базального отдела сердца направлен вправо, вверх, назад.
Последовательность сокращения миокарда можно оценить косвенно через хронологическую последовательность изменения геометрии камер сердца, используя возможности других диагностических методов (МРТ, ЭхоКС, тканевой допплерографии) и результатов, полученных экспериментальным путём.
Чётче понять последовательность сокращения миокарда позволяет сопоставление с изменением давления в камерах по фазам сердечного цикла.

Попробуем проследить кинематику сердца по фазам сердечного цикла.
Систола начинается с фазы асинхронного сокращения (АС) при замкнутых створчатых и полулунных клапанах, когда импульсы возбуждения достигают верхнего отдела перегородки и базальных слоёв желудочков. В эту фазу геометрия сердца и давление существенно не меняются. Исходя из этого, можно допустить, что сокращаются миофибриллы предсердно-желудочковой плоскости и самые высокие базальные отделы желудочков. Это позволяет сделать основание сердца более жёстким, клапанные кольца крепче фиксируются и, возможно, насколько сужаются. Таким образом, создаётся некий временный остов, к которому крепятся все остальные мышечные слои. Длится эта фаза приблизительно 55мс.
Фаза изометрического сокращения (IC) характеризуется тем, что за достаточно короткий промежуток времени (30мс) существенно изменяется геометрия сердца и значительно нарастает давление в камере левого желудочка (с 10-12 до 85-90мм.рт.ст.). Это наиболее динамичная фаза сердечного цикла, и объяснение этому следует искать в активной работе достаточно большой массы миокарда.
В норме при синусовом ритме правый желудочек сокращается несколько раньше левого, однако электрический импульс, достигнув первой группы мышц и возбудив её, продолжает распространяться как по межклеточным щелям, так и по проводящей системе сердца, поэтому электрическая активация распространяется на базальные отделы достаточно быстро.
В фазу изометрического сокращения последовательное сокращение правого и левого сегментов «полосы» приводит к плотному круговому охвату желудочков и увеличению внутриполостного давления. Эта часть работы выполняется мышечными слоями базального цикла. В эту фазу отмечается некоторое уменьшение внутреннего сечения желудочков, хотя и незначительное, поскольку камеры сердца заполнены слабо сжимаемой кровью при закрытых клапанах.
На данном отрезке времени возросшее давление может оказывать влияние на расслабленный миокард апикального цикла, увеличивая его в поперечнике и несколько растягивая сердце по длинной оси. Поэтому, несмотря на удлинение сосочковых мышц, хорды остаются в натянутом состоянии, и, следовательно, хорошо удерживают створки митрального клапана.
Не следует забывать и об субэпикардиальном слое, базальные отделы которого возбуждаются и сокращаются одновременно с циркулярными. Направление этих волокон параллельно продольной оси, поэтому при их сокращении будет возникать противодействие чрезмерному увеличению сердца по длинной оси. Кроме того, они, как на верёвках, будут прокручивать верхушку вправо, выпрямляя путь оттока.
Спустя 10-15мс возбуждение достигает нисходящего сегмента апикального цикла и верхушечного отдела субэпикардиального слоя, при одновременном сокращении которых происходит скручивание сердца (базальный отдел проворачивается против часовой, а верхушка по часовой стрелке). Это приводит к ещё большему уменьшению сечения сердца в поперечнике и приросту давления.
Аортальный клапан открывается после того, как давление в левом желудочке (≈85мм.рт.ст.) превысит давление в аорте.
С этого момента начинается фаза быстрого изгнания (Em). Несмотря на то, что произошла «разгерметизация» камер желудочков, давление продолжает нарастать и к концу фазы в левом желудочке достигает ≈130мм.рт.ст. В результате укорочения продольной оси камера левого желудочка превращается из овоидной в сферическую.
Всему этому есть только одно объяснение: к началу периода изгнания в работу включаются все слои миокарда. К задействованным ранее, добавляются восходящий сегмент апикального цикла и субэндокардиальный слой.
При совместном сокращении нисходящего и восходящего сегментов апикального цикла предсердно–желудочковая перегородка подтягивается к верхушке, что приводит их к взаимодействию по типу поршня с цилиндром. Однако парадокс заключается в том, что «цилиндр» движется в сторону «поршня», а не наоборот.
Несмотря на укорочение камеры сердца, сокращающиеся сосочковые мышцы удерживают хорды в напряжении, не позволяя пролабировать створкам митрального клапана.
Фаза быстрого изгнания длиться около 105мс и заканчивается на пике давление. За этот период изгоняется до 70% крови суммарного сердечного выброса.
Фаза медленного изгнания (Er) характеризуется прогрессирующим падением давления в желудочке при продолжающемся выбросе крови в аорту. К концу фазы оно снижается приблизительно до 90мм.рт.ст. При этом сердце, несколько укорачивается по длинной оси и расширяется в поперечнике.
Этому может быть такое объяснение: доминирует сила, формируемая мышечными сегментами апикального цикла, совместный вектор которых притягивает основание сердца к динамическому центру, укорачивая продольную ось. Падение давления совместно с некоторым расширением базального отдела следует связывать не только со снижением общей массы крови в желудочке, но и с переходом в расслабленное состояние некоторой части миокарда. В результате расслабления мышечных слоёв базального цикла уменьшается сопротивление данной области миокарда внутренним силам, что и служит объяснением некоторому растяжению камер сердца в поперечнике.
Продолжительность этой фазы приблизительно равна 150мс.
Протодиастола (Pr) начинает диастолу. Её продолжительность не превышает 40мс. В эту фазу между левым желудочком и аортой наступает гемодинамическое равновесие: сердечный выброс завершён, а клапан аорты ещё не закрылся. Для его закрытия необходимо снизить давление в камере сердца на 10-15 мм.рт.ст., что и происходит в протодиастолу.
Поскольку масса крови в желудочках остаётся неизменной, то для снижения её плотности необходимо увеличить объём самой камеры. Если нисходящий сегмент прекратит сокращаться, то сокращающийся самостоятельно восходящий сегмент апикального цикла начнёт раскручивать предсердно-желудочковую перегородку по часовой стрелке, что приведёт к некоторому увеличению базального отдела в поперечнике и приросту объёма камеры.
Фаза изометрического расслабления (IR) продолжается в течение 85мс при закрытых клапанах. Хочу сразу же заметить, что данный устоявшийся термин не согласуется с происходящими процессами и его следовало бы переименовать на фазу изометрического растяжения.
На этом этапе продолжается не только расширение камеры левого желудочка в базальном отделе, но и увеличение по длинной оси.
К началу этой фазы сокращаются только восходящий сегмент апикального цикла и субэндокардиальный слой. В результате их антагонистических действий продолжается раскручивание сердца (рис. IV-8).
А вот растягивание сердца по длинной оси, с моей точки зрения, следует связать с упруго-эластическими свойствами аорты и лёгочной артерии. После притока крови в систолу их упругость возрастает, а противодействие мышечных слоёв резко снижается. Вероятнее всего, это и является основным механизмом по возврату предсердно-желудочковой перегородки к своему исходному положению.
Фаза изометрического расслабления (растяжения) заканчивается открытием митрального клапана, когда давление в левом желудочке опускается ниже давления в левом предсердии (5-7мм.рт.ст.).
В фазу быстрого наполнения (Fr) кинематика левого желудочка осуществляется теми же силами, что и в фазу изометрического растяжения. Камеры сердца продолжают растягиваться в поперечнике и по длинной оси. Давление также постепенно снижается. В результате, создаётся разрежение и условия для поступления около 25мл крови из предсердия в желудочек по градиенту.
При достижении давления 3мм.рт.ст. активное растяжение левого желудочка прекращается, что, прежде всего, следует связать с расслаблением восходящего сегмента и субэпикардиального слоя миокарда. С этого момента все слои сердечной мышцы находятся в расслабленном состояния.
Эта фаза длиться приблизительно 110мс и после выравнивания градиента давления между левыми предсердием и желудочком заканчивается.
Кинематика в фазу медленного наполнения (Dy) осуществляется иными силами и процессами. Её правильнее назвать фазой преднагрузки, поскольку именно с последней связана дальнейшая трансформация левого желудочка.
Волна давления, сформировавшаяся систолой правого желудочка, пройдя через малый круг, достигает левого желудочка. Около 30мл крови, поступающей в левый желудочек под давлением порядка 10мм.рт.ст., растягивает его ещё больше во всех направлениях. Эта фаза длится приблизительно 175мс.
Сердечный цикл завершается систолой предсердий (Sa), когда под давлением порядка 12 мм.рт.ст. в левый желудочек нагнетается ещё около 12 мл крови.
В результате этого левый желудочек доводится до оптимального размера и полностью подготавливается для повторного сердечного цикла.
Систола левого предсердия заканчивается через 100мс закрытием митрального клапана.
Чтобы закрыть тему кинематики сердца, хотел высказать некоторые свои взгляды на предназначение весьма загадочно устроенного трабекулярного аппарата. Почему сердце изнутри выстлано не гладким слоем, а «изрыто оврагами и ямами».
Версия о том, что они предназначены для придания стенке большей крепости при растяжении, выглядит весьма сомнительно. Для этого имеются иные достаточно простые возможности, например, усиление соединительно-тканного каркаса, как у сосудов. Сердечная мышца сама наращивает давление в камерах сердца, и как саморегулирующийся орган, способна подстроить его под свои упруго-эластические свойства.
При сокращении некоторых слоёв миокарда происходит ротация базального отдела сердца в ту или иную сторону. Это может придавать крови некоторое вращение по спирали. Согласно законам гидродинамики, по сравнению с прямолинейным такой вид движения ведёт к большим затратам энергии. Возможно, продольно расположенные трабекулы выполняют задачу «прибрежных валунов», гасящих турбуленции и выталкивающих поток на «стремнину», где доминирует прямолинейное движение.
При изгнании крови во время систолы верхушка сердца выполняет функцию «поршня», проталкивая кровь в аорту. А почему бы не допустить, что многочисленные «карманы» на внутренней поверхности левого желудочка предназначены для той же цели.
В фазу медленного кровенаполнения происходит растяжение камеры левого желудочка под давлением поступающей крови (преднагрузка). Прямолинейно движущаяся кровь будет «упираться» в верхушку и растягивать желудочек по длинной оси. Возможно, многочисленные трабекулярные складки служат упором для растяжения сердца в поперечнике.
В связи с появившимися новыми диагностическими возможностями всё больше внимания уделяется оценке внутрисердечной асинхронии, то есть нарушению скоординированной работы отдельных участков миокарда, поскольку она сможет послужить маркером систолической и диастолической дисфункций сердца [11].
Вместе с этим доказано существование физиологической гетерогенности движения участков миокарда желудочков сердца у здоровых людей. Очевидно, что для определения патологического характера асинхронии миокарда необходимо знать пределы физиологической асинхронии.
 Согласно модели «скользящих нитей», сокращение мышцы происходит в результате перемещения (скольжения) толстых и тонких нитей в саркомере навстречу друг другу без изменения их длины [26,108]. Актиновые нити скользят вдоль параллельно расположенных миозиновых нитей, образуя межу собой циклические связи (cross bridge – перекрещивающиеся соединения), и, таким образом укорачивают саркомер, притягивая Z-пластинки друг к другу.
Согласно модели «скользящих нитей», сокращение мышцы происходит в результате перемещения (скольжения) толстых и тонких нитей в саркомере навстречу друг другу без изменения их длины [26,108]. Актиновые нити скользят вдоль параллельно расположенных миозиновых нитей, образуя межу собой циклические связи (cross bridge – перекрещивающиеся соединения), и, таким образом укорачивают саркомер, притягивая Z-пластинки друг к другу.
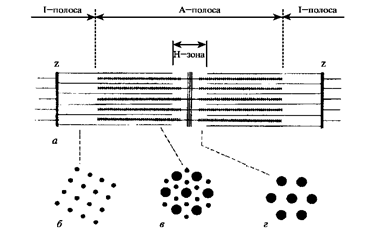
Рисунок IV-10. Схема расположения толстых и тонких нитей в саркомере поперечно-полосатой мышцы (по J. Squire, 1981).
На толстых нитях поперечной штриховкой выделена область, содержащая миозиновые выступы (мостики).
А — тонкая (актиновая) нить;
М — толстая (миозиновая) нить.
а) саркомер в продольном сечении,
б) поперечные срезы через участок саркомера вблизи Z-мембраны,
в) поперечные срезы через участок саркомера в области перекрытия толстых и тонких нитей,
г) поперечные срезы через участок саркомера в Н-зоне.
Скольжение нитей в сокращающейся мышце связывают с действием независимых генераторов силы, равномерно распределённых в саркомере между актиновыми и миозиновыми нитями и действующими циклически. В мостиковой модели такими генераторами силы принято считать выступающие из ствола толстой нити мостики тяжёлого меромиозина (миозиновые головки и субфрагмент 2).
Кардиомиоциты состоят из саркомеров, содержащих толстые и тонкие филаменты (нити), имеющие свойство взаимно скользить относительно друг друга.
Более толстые нити, диаметром около 15нм и длиной 1,5мкм, состоят, в основном, из миозина (рис. IV-11). На одном из концов молекулы миозина тяжёлые цепи расходятся, образуя две массивные грушевидные глобулярные головки (субфрагменты 1). Второй участок, присоединённый к головке, разделяет миозиновый стержень на две функционально различные части: лёгкий меромиозин и субфрагмент 2. Стержни лёгкого меромиозина плотно упакованы, образуя стволы нитей, тогда как субфрагменты 2 и глобулярные головки подвижны и способны участвовать в процессе взаимодействия с актиновыми нитями. В покоящейся мышце субфрагменты 2 прижаты к стволу таким образом, что глобулярные головки миозина, расположенные на поверхности, образуют своеобразную трёхтяжевую спираль. При активации мышцы субфрагменты 2 могут отходить от ствола, обеспечивая головкам возможность приближаться к актиновым нитям и взаимодействовать с ними.

Рисунок IV-11. Схематическое изображение молекулы миозина (по Rayment I., Holden H., 1994).
Более тонкие нити (рисунок IV-12), диаметром 8-10нм и длиной около 1мкм, состоят из актина и Са-чувствительных регуляторных белков — тропомиозина и тропонинов. Тропомиозин располагается в канавках актиновой спирали в виде двух тяжей. На тяжах тропомиозина с регулярными интервалами 36-38нм находятся комплексы тропонина.

Рисунок IV-12. Строение тонкой нити – актина ( по Ebashi S., 1975).

Рабочий цикл мостика. Способность к движению — одно из характерных свойств всех живых организмов. Все разнообразные формы проявления двигательной активности имеют общую черту - превращение химической энергии, освобождающейся при гидролизе АТФ, в механическую. Рабочий цикл мостика между актином и миозином также связан с гидролизом АТФ. Согласно современным представлениям, цикл гидролиза АТФ актомиозином в мышце (рабочий цикл мостика) можно условно разделить на 6 стадий (рисунок IV-13), отличающихся по структуре и химическим свойствам мостика:
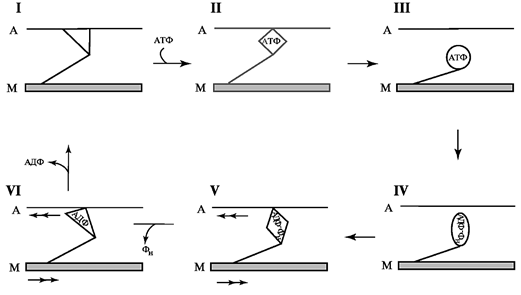
Рисунок IV-13. Рабочий цикл мостика (по R. R. Schroeder et al., 1992).
А — актиновая нить (глобулы актина не показаны); М — миозиновая нить; I-VI — последовательные стадии рабочего цикла. Изменения миозиновой головки условно показаны как изменения её геометрической формы.
III – IV стадии. Расщепление АТФ на АДФ и неорганический фосфат происходит на свободном (не связанном с актином) миозине. В покоящейся мышце мостики не взаимодействуют с актином, поэтому такая мышца, находящаяся в состоянии релаксации, легко растяжима.
IV-V стадии. Образовавшийся долгоживущий миозин-АДФ комплекс может соединяться с актином. Содержащая продукты биохимической реакции миозиновая головка подходит к актиновой нити и замыкается на одной из глобул в положении, перпендикулярном оси нити. Белок тропомиозин закрывает активные центры на тонкой нити. После присоединения свободного кальция к регуляторному белку тропонину-С активные центры актина переходят в открытое состояние, что создаёт условия для присоединения поперечных мостиков. В результате этого центры взаимодействия на глобулах актина становятся доступными для замыкания миозиновых мостиков. Структура толстых нитей при активации также изменяется; происходит разупорядочивание мостиков и их отход от ствола толстой нити по направлению к тонким.
V-VI стадии. Затем миозиновая головка поворачивается, наклоняясь на угол примерно 45°, и проталкивает актиновую нить в направлении от Z-мембраны (рабочий ход мостика).
VI-I стадии сбрасывания АДФ.
I стадия соответствует ригорному состоянию мостика, когда в мышце исчерпан АТФ и она становится нерастяжимой, что принято считать результатом замыкания максимального числа мостиков.
I—II стадии происходит связывание новой молекулы АТФ,
II—III стадии возникновение новой диссоциации мостика и начала нового рабочего цикла.
Мостики работают независимо друг от друга, т. е. сила, развиваемая отдельным мостиком, полностью определяется свойствами самого мостика. Силы, развиваемые отдельными мостиками, суммируются. При сокращении величина генерируемой мышцей силы зависит от длины саркомера, точнее от степени перекрытия актиновых и миозиновых нитей, т. е. она пропорциональна числу работающих мостиков.
И ещё, в нормальном сердце существуют различия между механическими свойствами отдельных кардиомиоцитов. Зависимость силы от длины саркомера в клетках субэндокарда больше, чем в субэпикарде, что обусловлено неодинаковой скоростью изменения сродства тропонина-С с кальцием в процессе активации сократительных белков. Были обнаружены три изоформы миозина: быстрая v1, неактивная v2, медленная v3, различным образом распределённые между миоцитами эпикарда и эндокарда.
С точки зрения биофизики, мостик замыкается в начале тянущей зоны и начинает развивать тянущую силу. Рабочий ход мостика жёстко связан со скольжением нитей. После окончания рабочего хода мостик переходит в тормозящее состояние, в котором он получает возможность разомкнуться. После размыкания мостик снова возвращается в исходное состояние.
 Управление сократительной активностью мышцы осуществляется с помощью большого числа мотонейронов, аксоны которых в составе двигательного нерва подходят к мышце. Войдя в мышцу, аксон разветвляется на множество веточек, расходящихся к разным волокнам. Таким образом, один мотонейрон иннервирует целую группу мышечных волокон (так называемая нейромоторная функциональная единица), которая работает как единое целое. Мышца состоит из множества функциональных единиц, которые возбуждаются и сокращаются не всей своей массой одновременно, а поэтапно с регулярной хронологической последовательностью в каждом сердечном цикле.
Управление сократительной активностью мышцы осуществляется с помощью большого числа мотонейронов, аксоны которых в составе двигательного нерва подходят к мышце. Войдя в мышцу, аксон разветвляется на множество веточек, расходящихся к разным волокнам. Таким образом, один мотонейрон иннервирует целую группу мышечных волокон (так называемая нейромоторная функциональная единица), которая работает как единое целое. Мышца состоит из множества функциональных единиц, которые возбуждаются и сокращаются не всей своей массой одновременно, а поэтапно с регулярной хронологической последовательностью в каждом сердечном цикле.
Скорость распространение возбуждения по клеткам зависит от уровня электропроводности межклеточного контакта. Во вставочных дисках между смежными клетками имеются высокопроницаемые межклеточные щелевые контакты (нексусы) с очень низким электрическим сопротивлением (рисунок IV-2). Все же, следует помнить, что по проводящей системе сердца (волокнам Пуркинье) скорость проведения импульса (4 м/сек) в 10 раз выше, чем по межклеточным контактам (0,3-0,5 м/сек). Это приводит к неодновременному возбуждению миокарда по типу «цепной реакции».
Возбуждение сердечной мышцы начинается после того, как стимул достигнет клетки миокарда. Волна возбуждения быстро распространяется вдоль сарколеммы через щелевые контакты и проникает внутрь клетки через тубулы.
Потенциал действия сердечной мышцы вызван активацией двух типов ионных каналов:
- Без ионов Na+ сердце невозбудимо, оно не станет биться, так как биопотенциал (потенциал действия) зависит от внеклеточных ионов натрия. В результате активации быстрых натриевых каналов внутрь мышечного волокна поступает огромное количество ионов натрия. Эти каналы остаются открытыми лишь несколько тысячных долей секунды.
- Медленные кальциевые каналы, которые также называют кальциево-натриевыми каналами, медленно открываются и, что особенно важно, долго остаются открытыми (в течение нескольких десятых долей секунды). Всё это время ионы кальция и натрия диффундируют внутрь сердечных волокон и поддерживают длительную деполяризацию мембраны, образуя фазу плато потенциала действия. Наличие этой фазы способствует увеличению продолжительности периода сокращения желудочков в 15 раз по сравнению со скелетной мышцей.
Более того, свободные ионы Са++ внутри клетки являются важнейшим фактором, влияющим на сократительную способность миокарда. Снижение ионов Са++ во внеклеточной жидкости приводит к уменьшению силы сердечных сокращений и возможной остановке сердца в диастоле. Напротив, повышение их концентрации увеличивает силу сердечных сокращений и может привести к остановке сердца в систоле.
Во второй фазе (время плато) потенциала действия повышается проницаемость сарколеммы для Са++. Он входит в клетку по электрохимическому градиенту через кальциевые каналы сарколеммы и её инвагинаций (Т-системы). Количества кальция, вошедшего внутрь клетки из внеклеточного пространства, недостаточно для того, чтобы вызвать сокращение миофибрилл. Он скорее выполняет роль триггера, запускающего высвобождение ионов Са++ из саркоплазматического ретикулума, где есть его запас в связанном состоянии. Саркоплазматический ретикулум представляет собой систему сплюснутых вытянутых соединяющихся друг с другом пузырьков, которые охватывают каждый саркомер миофибриллы, подобно муфте (рисунок IV-2). Части саркоплазматического ретикулума, прилегающие к поперечным трубочкам (терминальные цистерны), образуют с окончаниями поперечных трубочек специализированные контакты — триады.
Концентрация Са++ в клетке возрастает в 10-100 раз, после чего он связывается с белком тропонином-С. Кальциево-тропониновый комплекс снимает блок с активных участков между актиновыми и миозиновыми филаментами, вызванный тропомиозином, что позволяет образовывать поперечные циклические связи (cross bridges) между ними и, следовательно, сокращаться миофибриллам.
 После окончания сокращения приток Са++ в клетку прекращается, саркоплазматический ретикулум начинает активно поглощать Са++ благодаря кальциевому насосу, который работает с использованием энергии АТФ (ATP-energized Ca++ pump). К тому же фосфорилирование тропонина-I подавляет связывание Са++ тропонином-С. Этот процесс позволяет тропомиозину снова заблокировать участки взаимодействия актиновых и миозиновых нитей, что приводит к расслаблению.
После окончания сокращения приток Са++ в клетку прекращается, саркоплазматический ретикулум начинает активно поглощать Са++ благодаря кальциевому насосу, который работает с использованием энергии АТФ (ATP-energized Ca++ pump). К тому же фосфорилирование тропонина-I подавляет связывание Са++ тропонином-С. Этот процесс позволяет тропомиозину снова заблокировать участки взаимодействия актиновых и миозиновых нитей, что приводит к расслаблению.
Са++, поступивший из внеклеточного пространства, должен быть удалён из клетки во время расслабления. Обратный транспорт кальция из цитозоля (так называемая секвестрация) осуществляется, прежде всего, за счёт Na+/Ca++ обменника в пропорции 3 иона натрия на 1 ион кальция. Кальций также удаляется из клетки электрогенным насосом, который использует энергию АТФ для переноса Са++ через сарколемму (Ca++ pump).
Когда медленные кальциевые каналы закрываются (через 0,2-0,3сек) и прекращается входящий ток ионов кальция и натрия, быстро возрастает проницаемость мембраны для ионов калия, что ведёт к быстрому возврату мембранного потенциала к состоянию покоя. Снижение концентрации внеклеточных ионов K+ не оказывает большого влияния на возбуждение и сокращение сердечной мышцы. Однако увеличение внеклеточного калия до достаточно высоких уровней вызывает деполяризацию с потерей возбудимости клеток миокарда и остановку сердца в диастоле.
Основными задачами, стоящими перед сердцем, являются доставка кислорода и других продуктов жизнедеятельности к тканям и распределение жидкости по органам и системам.
Общая вода организма составляет около 60% массы тела. Она распределена между внеклеточным, внутриклеточным и внутрисосудистым пространством в пропорции: около 12 л (27%) интерстициальной жидкости, около 30 л (67%) внутриклеточной жидкости и около 3 л (6%) плазмы. Для того чтобы обеспечить её полное обновление в тканях, величина объёма жидкости, диффундирующей из кровяного русла в ткани и обратно должна превышать величину минутного объёма крови, выбрасываемой сердцем, примерно в 45 раз (Pappenheimer, 1953 г.). Тканевая жидкость обновляется непрерывно; даже в областях с наименьшей капиллярной сетью её полное обновление осуществляется менее чем за 30 минут (Elkinton, 1955 г.).
Сердечная мышца непрерывно сокращается в течение жизни и требует постоянного снабжения кислородом. Поэтому она содержит очень много митохондрий. Митохондрии содержат энзимы, необходимые для окислительного фосфорилирования, и отвечают за быстрое окисление субстратов при синтезе АТФ с целью удовлетворения энергетических потребностей миокарда (рисунок IV-2).
Миокард также щедро снабжён капиллярами: на одно мышечное волокно их приходится 6, 8 и более, что позволяет существенно ускорить обменные процессы. Обмен с капиллярами клетка осуществляет через структуру системных тубул (Т-система), которые представляют собой инвагинации сарколеммы внутрь кардиомиоцита.
Расслабление является для сердца не менее важной функцией, чем сокращение. Релаксация мышцы (её возвращение в состояние покоя) определяется уходом ионов Са++ в эндоплазматический ретикулум из саркоплазмы.
 Миокард состоит из поперечнополосатых мышц, но ни одна поперечнополосатая мышца не способна сама себя растянуть при расслаблении [32]. Возврат саркомера к изначальной длине чаще всего связывают с упруго-эластическими свойствами соединительнотканного каркаса миокарда, поэтому остановимся на нём более подробно.
Миокард состоит из поперечнополосатых мышц, но ни одна поперечнополосатая мышца не способна сама себя растянуть при расслаблении [32]. Возврат саркомера к изначальной длине чаще всего связывают с упруго-эластическими свойствами соединительнотканного каркаса миокарда, поэтому остановимся на нём более подробно.
При изучении морфологии сердца в его структуре выделяют два компонента: мышечный, в виде кардиомиоцитов, и «немышечный» или соединительнотканный. Последний представлен прослойками рыхлой волокнистой соединительной ткани с проходящими в ней сосудами и нервными элементами.
Объёмный баланс кардиомиоцитов (паренхимы) и соединительнотканного компонента (стромы) в миокарде колеблется в соотношении 4:1 (80% и 20%)
Соединительнотканный компонент миокарда представлен клетками и межклеточным веществом (в современной литературе для межклеточного вещества чаще используется синоним «внеклеточный матрикс», extracellular matrix), в котором выделяют аморфный и волоконный компоненты. Кардиомиоциты и соединительнотканные клетки окружены межклеточным веществом.
- В количественном отношении в строме миокарда преобладают клеточные элементы соединительной ткани (65 - 75%). Среди клеток наиболее часто встречаются фибробласты (90 - 95%) и тучные клетки (4 - 9%). Фибробласты являются основными продуцентами макромолекул матрикса, включая коллаген и главные структурные белки. Остальные клеточные формы представлены тучными клетками, макрофагами, лимфоидными клетками.
- Основное, или аморфное вещество полианионной природы обеспечивает трофическую и метаболическую функции.
- Коллагеновые и эластические волокна межклеточного вещества образуют своеобразный каркас для кардиомиоцитов, имеющий сложную пространственную организацию, постоянно изменяющий свою форму во время сердечного цикла. Одним из основных факторов, определяющих архитектонику волокон, является сила и распределение действующих на ткань нагрузок, которые меняются в зависимости от фазы сердечного цикла.
Морфологическая и функциональная гетерогенность соединительнотканного компонента миокарда позволяет выделить в его составе эпимизий, перимизий и эндомизий, которые отличаются друг от друга по составу, пространственной организации входящих в них элементов и локализации.
Эпимизий представляет собой прослойку соединительной ткани, окружающую весь миокард по эпикарду и эндокарду. Основными компонентами эпимизия являются пучки коллагеновых волокон, достигающие в диаметре нескольких микрометров.
Эндомизий покрывает каждое мышечное волокно в виде сетчатого футляра из коллагеновых волокон (диаметром 30 - 70нм). Эти волокна собираются в небольшие тяжи - «распорки» (диаметром 120 - 150нм), которые закрепляются в базальной мембране кардиомиоцитов между фестонами сарколеммы на уровне Z-дисков. Направляясь от одного волокна к другому перпендикулярно длинной оси клетки, коллагеновые волокна объединяют их в пучок. Считается, что коллагеновые «распорки» эндомизия сохраняют в течении сердечного цикла необходимое расстояние между кардиомиоцитами и продольное направление капилляров. Коллагеновые волокна, окружающие мышечные волокна, располагаются по их длине с интервалом 5 - 6 мкм.
Перимизий представлен пучками коллагеновых волокон, которые соединяют волокнистые элементы эндомизия и эпимизия, формируя каркас для группы мышечных волокон. В перимизии коллагеновые волокна образуют толстые извитые пучки, которым приписывают роль демпферной системы, защищающей кардиомиоциты от чрезмерного растяжения. Извитость этих пучков максимальна во время систолы и уменьшается во время диастолы.
Составляющая основу межклеточного вещества сеть коллагеновых и эластических волокон связывает в единое целое компоненты миокарда, сохраняет нужную сердечной мышце форму и определяет механические свойства миокарда во время сердечного цикла. Из фибриллярных белков преобладают коллаген I и коллаген III типов. Около 80% всего коллагена представлено коллагеном I типа, входящего в состав нерастяжимых толстых волокон миокарда, обеспечивающих его прочность. Около 11% приходится на коллаген III типа, с которым связывают растяжимость миокарда. Соотношение коллагенов I и III типов в нормальном миокарде достаточно стабильно и может считаться одной из основных характеристик межклеточного вещества миокарда.
Толстые коллагеновые волокна располагаются преимущественно в перимизиальных прослойках. Направление этих волокон совпадает с направлением кардиомиоцитов, а длина и извитость изменяются с фазами сердечного цикла. Этим волокнам приписывают роль в сохранении целостности саркомеров кардиомиоцитов при увеличении кровенаполнения камер сердца. Степень волнообразной извитости этих волокон уменьшается по мере нарастания диастолического давления в камерах сердца.
Разновидностью фибробластов являются миофибробласты, сочетающие в себе качества фибробласта и гладкого миоцита. Миофибробластам приписывается способность динамического изменения объёма межклеточного вещества, а также влияние на ориентацию его волокнистых элементов. Увеличение количества миофибробластов наблюдается при различных склеротических процессах в сердце.
Упруго-эластичные свойства того или иного материала заложены в молекулярной структуре. Это две взаимодополняющие физические и физиологические категории, поэтому они никогда не оцениваются раздельно.
Хочу напомнить, упругость - свойство тела противодействовать деформации под внешним воздействием, растяжимость - поддаваться деформации (величина обратная упругости); эластичность сосудов - это способность возвращаться к первоначальному состоянию после их растяжения (пластичность - свойство обратное эластичности).
Обладает ли упруго-эластичными свойствами миокард? Вне всякого сомнения, обладает. Но достаточно ли этих сил для возвращения филаментов всего миокарда в исходное состояние при расслаблении кардиомиоцитов в диастолу?
Подсчитаем. В общей массе здорового миокарда имеется 80% кардиомиоцитов и 20% стромы. Филаменты кардиомиоцитов нерастяжимы. Строма на 70% состоит из клеточных элементов. Следовательно, в общей массе миокарда аморфное вещество и соединительнотканные волокна составляют около 6%. Если принять, что они представлены в межклеточном веществе поровну, то количество соединительнотканных волокон в общей массе миокарда не превышает 3%. Среди них около 80% представлено нерастяжимым коллагеном I типа. И только 11% приходится на коллаген III типа, с которым связывают растяжимость миокарда. Итого, количество соединительнотканных волокон, обладающих упруго-эластическими свойствами, не превышает 0,3 – 0,5%. Даже если сделать поправку на некоторое участие других тканей в этом процессе, то эта цифра едва ли превысит 1%.
Для сравнения, упругие свойства стенок сосудов определяются волокнами трёх типов - эластическими, коллагеновыми и гладкомышечными. Эластин является резиноподобным материалом, модуль Юнга которого равен примерно 3*105 Н⋅м-2. Коллаген гораздо более жёсткий, чем эластин, его модуль Юнга равен примерно 1*108 Н⋅м-2. Модуль Юнга у гладкомышечного волокна примерно такой же, как и у эластина, однако в зависимости от физиологической активности он может меняться от 1*105 до 2*106 Н⋅м-2.
Упруго-эластические свойства стенок аорты и крупных магистральных сосудов представлены так: на долю эластина и гладких мышц приходится около 35% и 25% сухого веса соответственно, а доля нерастяжимого коллагена не превышает 15-20% сухого вещества.
Как видите, разница несоизмерима. Миокард не создавался как упруго-эластичный орган, а участие некоторых тканей в этом процессе имеет локальные узконаправленные задачи.
Участвует ли соединительнотканный каркас сердца в растяжении расслабленного миокарда? Возможно, доля его участия в этом есть, но с уверенностью можно сказать, что этих сил явно недостаточно для полноценного проведения диастолы.
Природа создавалась Творцом по «идеальному проекту». Всё в ней базируется на оптимальной целесообразности. Именно с этих позиций мы должны рассматривать не только весь человеческий организм, но и любую его часть. Тем более, когда речь идёт о сердце, в котором все процессы рассчитаны до миллисекунд. Едва ли в нём для выполнения какой-либо задачи может быть использован остаточный принцип.
Итак, давайте оценивать сердце как «идеально» сформировавшийся орган. В нём всё - ткани, форма, химический состав, функции - сопоставлено так, чтобы орган работал в наиболее оптимальном режиме.
Миокард не планировался и не создавался как упруго-эластичный орган по той же причине, по которой поршень в цилиндре не делают из мягкой резины. Такой двигатель менее эффективен в работе, поскольку во время компрессии в камере увеличиваются затраты энергии на растяжения самого поршня. Именно по этой причине в миокарде использована не эластичная гладкая мускулатура, а нерастяжимая поперечно-полосатая мышечная ткань.
 Миокард состоит из поперечнополосатых мышц, но ни одна поперечнополосатая мышца не способна сама себя растянуть при расслаблении. Для поиска способов растяжения попробуем исходить из аналогии. Какие же механизмы используются в других системах для растяжения мышц данного типа? На конечностях у любой поперечнополосатой мышцы есть мышца-антагонист, сокращение которой и вызывает растяжение расслабившейся мышцы [134,135,136,137,138]. Возможно, природа использовала этот принцип и для миокарда?
Миокард состоит из поперечнополосатых мышц, но ни одна поперечнополосатая мышца не способна сама себя растянуть при расслаблении. Для поиска способов растяжения попробуем исходить из аналогии. Какие же механизмы используются в других системах для растяжения мышц данного типа? На конечностях у любой поперечнополосатой мышцы есть мышца-антагонист, сокращение которой и вызывает растяжение расслабившейся мышцы [134,135,136,137,138]. Возможно, природа использовала этот принцип и для миокарда?

Рисунок IV-14. Последовательность сокращения и расслабления слоёв миокарда
Для того чтобы мышечные слои действовали антагонистически необходимы два условия:
- Волокна слоёв должны быть разнонаправленными и неравными по силе.
- Сокращение мышечных волокон разных слоёв должно происходить асинфазно.
На предложенной схеме (рис. IV-14) показана последовательность сокращения и расслабления мышечных слоёв по фазам сердечного цикла.
Миофибриллы базального цикла, включающие правый и левый сегменты, сокращаются от начала систолы до окончания фазы быстрого изгнания. Всё остальное время они находятся в расслабленном состоянии и готовы к растяжению.
Несколько позже начинают сокращаться мышечные слои апикального цикла, волокна которого имеют отличное от базального слоя направление, и их расслабление наступает позже. В фазу медленного изгнания совместными действиями восходящего и нисходящего сегментов предсердно-желудочковая перегородка подтягивается к верхушке. Это ведёт к приросту плотности крови, которая распределяется давлением по всей внутренней поверхности желудочка. В местах, где миофибриллы базального слоя расслабились, возрастает трансмуральное давление в пользу внутренних сил, что ведёт к выдавливанию стенки кнаружи и растяжению мышечных волокон данного слоя.
Мышечный слой нисходящего сегмента начинает сокращаться раньше восходящего. В результате этого в фазу изометрического сокращения происходит прокручивание предсердно-желудочковой перегородки против часовой стрелки. В период изгнания данный слой совместными действиями с восходящим сегментом подтягивает базальную перегородку к верхушке.
К началу диастолы нисходящий сегмент приходит в расслабленное состояние. Продолжающий сокращаться восходящий сегмент раскручивает, а потому и растягивает мышечные волокна нисходящего сегмента. В этом процессе, возможно, принимают участие аорта и лёгочная артерия, через упруго-эластичные свойства которых, сердце растягивается по длинной оси. Некоторое растяжение волокон данного слоя возможно и в начале фазы изометрического сокращения, когда несколько раньше начавшие сокращаться мышечные волокна базального цикла под давлением отдаляют верхушку от основания, растягивая сердце по длинной оси.
Субэпикардиальный слой возбуждается неодновременно. Базальные его отделы противодействуют перерастяжению сердца по длинной оси, вызванному сокращением мышечных волокон базального цикла. В фазу изометрического сокращения апикальный отдел субэпикардиального слоя совместно с нисходящим сегментом участвует в скручивании сердца, проворачивая верхушку по часовой стрелке. В некоторой степени, одновременно с субэндокардиальным слоем, эта группа мышечных волокон участвует в подтягивании основания к верхушке в период изгнания.
Заканчивает сокращаться этот слой в конце периода изгнания. Растяжение его базального отдела осуществляется совместно с мышечными волокнами базального цикла при подтягивании основания к верхушке слоями апикального цикла. Антагонистом для верхушечного отдела данного слоя, вероятнее всего, служит субэндокардиальный слой, продолжающий сокращаться после расслабления субэпикардиального слоя. В начале диастолы его растяжение происходит через раскручивание верхушки сердца субэндокардиальным слоем против часовой стрелки.
Восходящий сегмент совместно с нисходящим активно участвует в выталкивании крови из левого желудочка на протяжении всего периода изгнания, подтягивая основание к верхушке. После наступления диастолы и расслабления нисходящего сегмента данная группа мышечных волокон продолжает своё сокращение, раскручивая сердце совместно с субэндокардиальным слоем. Это приводит к увеличению камер сердца и снижению в них давления.
Субэндокардиальный слой прокручивает верхушку против часовой стрелки при раскручивании базального слоя по часовой стрелке восходящим сегментом. Этот слой в некоторой степени служит антагонистом субэпикардиальному, однако основной его задачей является стабилизация верхушки при сокращении восходящего сегмента. Поэтому они, вероятнее всего, начинают и заканчивают сокращение одновременно.
Оба этих слоя приходят к расслаблению в фазу быстрого наполнения, что совпадает с моментом снижения давления в левом желудочке до минимального уровня.
К началу фазы медленного кровенаполнения (Dy, диастазис) давление в левом предсердии и левом желудочке выравниваются. С этого момента расслабленные восходящий сегмент апикального цикла и субэндокардиальный слой готовы к растяжению, а вот антагонистических мышц для их растяжения нет. Из этого вытекает, что в процесс растяжения включаются иные механизмы.
Полученные результаты показывают, что мышечные слои, образующие стенки желудочков, функционируют асинфазно и начало диастолы (протодиастолы, фазы изометрического растяжения и быстрого наполнения) осуществляется активным сокращением некоторых мышечных слоёв.
И ещё, с моей точки зрения, поскольку между мышечными слоями существует весьма условная градация, поэтому сокращение миокарда происходит не так ступенчато, как указано на схеме, а, вероятнее всего, лавинообразно. Расслабление, надо полагать, происходит по аналогичной схеме.
Имеется два периода, на которые хотелось обратить внимание. Первый совпадает с периодом максимального изгнания, в котором все слои мышц находятся в сокращённом состоянии.
Второй совпадает с фазами медленного кровенаполнения и систолы предсердий, когда все слои миокарда находятся в расслабленном состоянии. Для того, чтобы восходящий сегмент апикального цикла и субэндокардиальный слой были растянуты до исходного состояния, должна быть задействована какая-то дополнительная сила. Поскольку в этот период все мышцы находятся в расслабленном состоянии, то единственной возможной силой, используемой для этой цели, может служить преднагрузка.

Под преднагрузкой понимают дополнительный потенциал, полученный сердечной мышцей в диастолу, при поступлении в левый желудочек объёма крови под некоторым давлением.
В момент открытия митрального клапана давление в левом предсердии равно 5-7 мм.рт.ст. В фазу быстрого наполнения восходящий сегмент апикального цикла и субэндокардиальный слой продолжают сокращаться, создавая присасывающий эффект. Давление в левом желудочке падает до своего минимума 2-3 мм.рт.ст., сокращение мышц прекращается, однако кровь продолжает наполнять желудочек, используя градиент давления между камерами. В эту фазу левый желудочек принимает около 40% поступающей крови. После выравнивания давления в камерах (0 градиент давления) приток крови должен прекратиться.
Однако наполнение левого желудочка продолжается и в фазу медленного кровенаполнения при расслабленных мышцах. Такое возможно только, если между камерами вновь появляется градиент давления, возникающий либо через снижение давления в камере притока, либо из-за возрастания его в камере оттока.
Поскольку первый вариант отпадает, то нам необходимо иметь доказательства возросшего давления в левом предсердии к данному моменту.
Итак, меняется ли давление в левом предсердии по фазам? Да, меняется.
На кривой оценивающей давление заклинивания лёгочной артерии (рис. IV-15) чётко видна пульсация, а ДЗЛА является эквивалентом давления в левом предсердии с поправкой на минус 2-3 мм.рт.ст. Итак, пиковое давление в левом предсердии может достигать 12-13 мм.рт.ст.

Рисунок IV-15. Нормальные значения давления и форма кривой при оценке ДЗЛА с помощью катетера Свана-Ганца.
Среднее давление в капиллярах малого круга кровообращения приблизительно равно 6,5 мм.рт.ст. Однако на максимуме выброса правого желудочка оно также возрастает. Значит кровоток в капиллярах пульсирующий. Хочу напомнить, что кроме поперечной, есть ещё и продольная пульсовая волна, характеризующаяся участками уплотнения и разрежения текущей крови. Вероятнее всего, преимущественно продольная пульсовая волна проходит через капиллярную сеть малого круга кровообращения, изменяя давление в левом предсердии по фазам.
Ещё один путь передачи пульсовой волны – артериовенозные анастомозы. Они используются в качестве «аварийных клапанов» сброса давления, минуя капиллярное русло. Даже в норме через открытые артериовенозные анастомозы проходит 2 - 4% ненасыщенной кислородом крови.
Средняя скорость распространения пульсовой волны по сосудам малого круга кровообращения относительно невелика - примерно 1,5-2 м/с. Кроме того, природа предусмотрительно сместила время сокращения правого желудочка по отношению к левому. Систола правого желудочка заканчивается на 30 мс позже, когда в левых камерах уже наступает диастола (рисунок V-7). Поэтому пик максимального давления приходит в левое предсердие в фазу медленного кровенаполнения левого желудочка.
Кровь, поступающая под напором, растягивает миокард, преодолевая некоторое сопротивление, в результате чего давление в желудочке прирастает на 3-4 мм.рт.ст. и вливается ещё около 40-50% поступающей крови.
Заканчивается период наполнения систолой предсердий (Sa). Несмотря на то, что в эту фазу поступает не более 15-20% от общего объёма необходимой крови (около 12 мл), следует учитывать то, что при сокращении предсердий саркомер доводится до оптимальной длины (2,2 мкм), тем самым наращивается его сократительный потенциал. Конечное диастолическое давление (КДД) в левом желудочке возрастает до 10-12 мм.рт.ст. Систола предсердий и вся диастола заканчивается закрытием митрального клапана.
В нормальном сердце наибольшая сила может быть достигнута при наполняющем давлении около 12 мм.рт.ст. При таком внутрижелудочковом диастолическом давлении, которое близко к верхнему пределу нормы, саркомер достигает длины 2,2 мкм. При дальнейшем подъёме давления в левом желудочке потенциальная сила миокарда перестаёт нарастать.
Предел растяжения саркомера равен 2,6 мкм. Эта способность миокарда сопротивляться растяжению при высоких значениях наполняющего давления обеспечивается за счёт несокращаемых компонентов сердца (соединительной ткани). Хочу заметить, что предельные цифры растяжения получены экспериментальным путём на изолированной мышце. Однако в живом организме даже при самых критических состояниях саркомер едва ли может быть растянут более 2,3 мкм.
Развиваемая сердечной мышцей сила максимальна, когда она начинает сокращение при длине саркомера в диапазоне от 2,1 до 2,2 мкм, при которой в состоянии покоя достигается оптимальное взаимное перекрытие толстых и тонких нитей, и количество перекрещивающихся соединений максимально.
Зависимость между начальной длиной волокон миокарда (или начальным объёмом) и силой (или давлением), развиваемой желудочком, иллюстрируют соотношение Франка-Старлинга (закон сердца Старлинга).
.
Конец IV раздела.

























